- Mapa conceptual de sistemas materiales
- ¿Cómo podemos obtener sustancias puras?
- Mapa conceptual de métodos de separación de mezclas
Bloque 1: Estructura atómica
- ¿Todo está hecho de átomos?
- Naturaleza de la materia.
- Estructura atómica.
- Configuración electrónica:
- Establece la distribución de los electrones en los diferentes ORBITALES. Los orbitales son regiones del espacio que rodea al núcleo en las que tenemos una elevada probabilidad de encontrar a un electrón.
- En cada orbital sólo puede haber un máximo de 2 electrones, con lo que puede estar vacío, con 1e o con 2e.
- Los orbitales son de 4 tipos:
- s : van de uno en uno, por lo que el nº máximo de electrones será de 2.
- p : van de tres en tres, por lo que el nº máximo de electrones será de 6
- d : van de cinco en cinco. Nº máximo = 10 electrones.
- f : van de siete en siete. Nº máximo = 14 electrones.
- Los orbitales se llenan de menor energía a MAYOR energía (de abajo a arriba). Siguiendo el anterior diagrama, encontraremos el siguiente orden: 1s2, 2p6, 3s2, 3p6, 4s2, 3d10, ....
- Con esta animación construiremos todas las configuraciones electrónicas de cualquier elementos. Observa cómo se va reproduciendo el diagrama de las flechas (diagrama de Moeller)
3. Animaciones
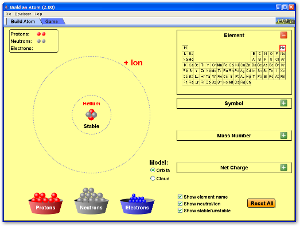
Construye un átomo
Otro constructor de átomos. Educaplus
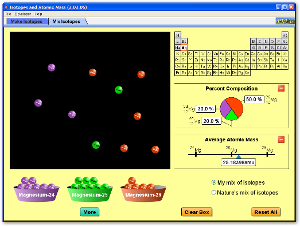
Isótopos y masa atómica
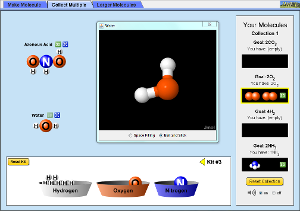
Construye una molécula
Bloque 2: Sistema periódico
1. Contenidos- ¿Por qué hay que estudiar el sistema periódico de los elementos?
- Web dinámica con una enorme cantidad de datos para trabajar en clase...
- ¿Todas los sistemas periódicos fueron siempre iguales?
- Impresora:
3. Animaciones
Bloque 3: Enlace químico
1. Contenidos- Enlace químico: web de CNICE premiada, con actividades.
- Mapas conceptual con enlaces a vídeos (1)
- Una estupenda imagene que relaciona enlace y tipo de compuestos.
2. Actividades
3. Animaciones








No hay comentarios:
Publicar un comentario
No copies contenidos de la Red.
Infórmate, cita las fuentes, extrae tus conclusiones, construye tus argumentos, organiza tu conocimiento....
Recuerda:PIENSA POR TI MISMO O MISMA.....SI NO LO HACES, OTROS PENSARÁN POR TI.